Gehaltsbestimmung von wirksamen Cannabis-Inhaltstoffen mittels HPLC nach DAB Monographie „Cannabisblüten“
Im Deutschen Arzneibuch 2018 (DAB 2018) veröffentlicht das Bundesinstitut für Arzneimittel und Medizinprodukte (BfArM) eine revidierte Monographie „Cannabisblüten“ (Cannabis flos).[1] Da das Europäische Arzneibuch (Ph. Eur.) keine entsprechende Monographie enthält, stellt die im DAB 2018 beschriebene Methode zur Gehaltsbestimmung von wirksamen Bestandteilen in Cannabisblüten mittels HPLC die EU-weit verbindliche Methode dar.[2] Die Monographie stellt die anerkannte pharmazeutische Regel nach Arzneimittelgesetz dar und wird bei Entscheidungen der zuständigen Behörden mit herangezogen.
Methode und Bedingungen
Die Auftrennung der laut DAB-Monographie zu bestimmenden Komponenten
– Cannabidiolsäure (CBDA),
– Cannabidiol (CBD),
– Cannabinol (CBN),
– Δ9-Tetrahydrocannabinol (THC) und
– Δ9-Tetrahydrocannabinolsäure (THCA)
wird auf einer Shim-pack Velox SP-C18 Trennsäule durchgeführt und auf der kompakten HPLC Nexera-i Plus umgesetzt. Die analytischen Bedingungen sind in Tabelle 1 zusammengefasst.

| Tabelle 1: analytische Bedingungen | |
|---|---|
| System | Nexera-i 3D plus |
| Säule | Shim-pack Velox SP-C18; 2.7 μm; 150x3.0 |
| Vorsäule | Shim-pack Velox SP-C18; 2.7μm; 5x3.0 (G) |
| Mobile Phase | A: Wasser + Phosphorsäure 85% (8.64 g/l) | B: Acetonitril |
| Gradient | 0 min 64% B, 16 min 82% B, 17-20min 64% B |
| Detektion | UV 225 nm (CBD, CBN, THC) | UV 306 nm (CBDA, THCA) |
| Flussrate | 1 ml/min |
| Inj.Volumen | 10 μL |
| Dauer | 20 min |
Gehaltsbestimmung
Die Herstellung der Standardlösungen und die Probenaufarbeitung erfolgt mit dem in der Monographie beschriebenen Verfahren:
Für die Probenaufarbeitung werden 0,500 g pulverisierte Droge 15 min lang mit 20 ml Ethanol 96 % geschüttelt und anschließend zentrifugiert. Der klare Überstand wird in einen 50-ml-Messkolben überführt. Der Rückstand wird 2-mal mit je 12,5 ml Ethanol 96 % gleichermaßen behandelt. Die organischen Lösungen werden zusammengeführt und mit Ethanol 96 % R zu 50,0 ml ergänzt. Diese Lösung wird durch ein Membranfilter aus regenerierter Cellulose von 0,45 μm nominaler Porenweite filtriert. 1,0 ml Filtrat wird mit Ethanol 96 % zu 10,0 ml ergänzt. [1]
Aus den Standardsubstanzen werden 5 Referenzlösungen der einzelnen Wirkstoffe in Methanol hergestellt. Für die Kalibration werden mindestens 6 Kalibrationslösungen aus den Referenzlösungen hergestellt, wobei jeweils eine definierte Konzentration zwingend gefordert wird (Tabelle 2).
| Substanz | Referenzlösung [mg/100ml] | Kalibration [μg/ml] | Muss Standard [μg/ml] |
|---|---|---|---|
| CBDA | 15 | 0,5 - 100 | 50 |
| CBD | 10 | 0,5 - 75 | 10 |
| CBN | 10 | 0,1 - 10 | 1 |
| THC | 10 | 0,5 - 75 | 10 |
| THCA | 30 | 0,5 - 250 | 50 |
Tabelle 2: Konzentration der Standards
Eignungsprüfung
Für die Eignungsprüfung wird eine weitere Referenzlösung aus Δ9-Tetrahydrocannabinol und Δ8-Tetrahydrocannabinol hergestellt. Die Auflösung zwischen beiden Peaks muss mindestens 1.2 betragen. Die Reproduzierbarkeit der Flächenwerte wird durch eine 6- fach-Injektion der THCA-Referenzlösung bei RSD < 1% belegt.
Kalibration
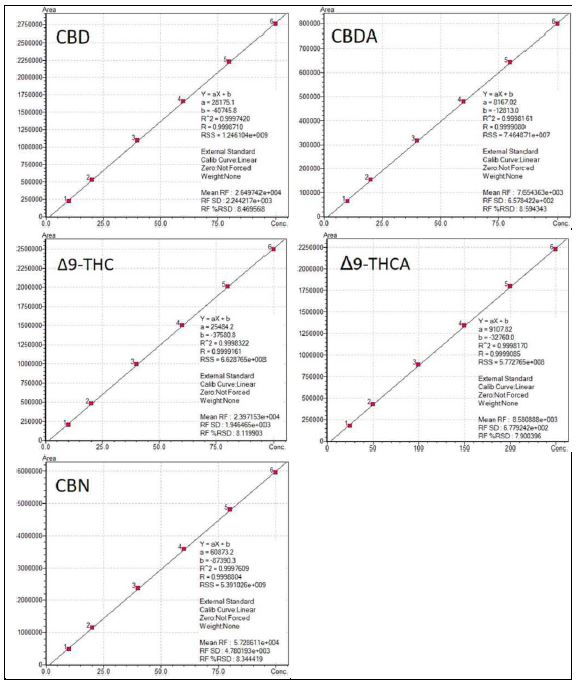
Für die Kalibration werden mindestens 6 Kalibrationspunkte der jeweiligen Substanzen nach Tabelle 2 gemessen. Die Auftragung der Peakflächen erfolgt gegen die Konzentration und wird linear gefittet (Abbildung 1).
Messung von Realproben
Es wurde Cannabis-Sorten aller 3 in der Monographie klassifizierten Produktgruppen (Tabelle 3) aufgearbeitet und mit der hier beschriebenen Methode gemessen (Abbildung 2 – 4). Die Auswertung erfolgte für das CBD, CBN und THC bei 225 nm und für das CBDA und THCA bei 306 nm.
| Produktgruppe | Gehalt an |
|---|---|
| I | Δ9-Tetrahydrocannabinol >> Cannabidiol |
| II | Δ9-Tetrahydrocannabinol ≈ Cannabidiol |
| III | Δ9-Tetrahydrocannabinol << Cannabidiol |
Tabelle 3: Klassifizierung der Produktgruppen
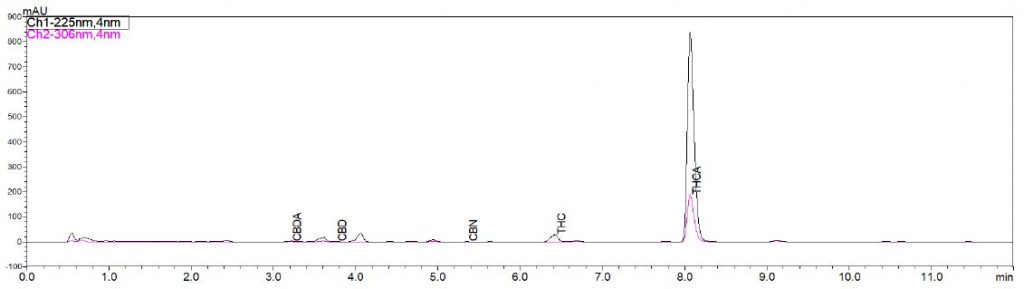
Abbildung 2: Chromatogramm von Cannabis der Produktgruppe I
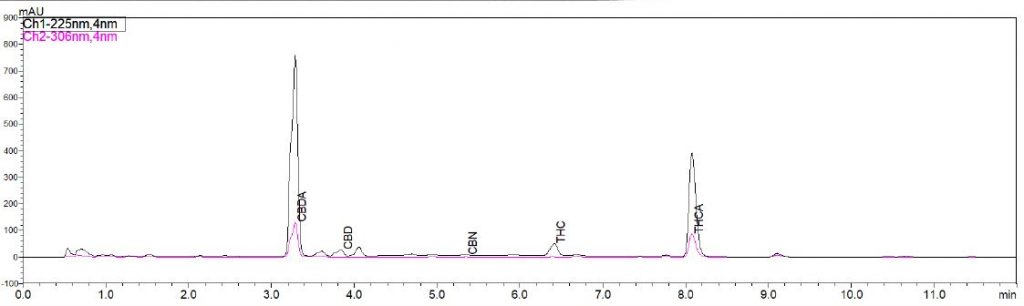
Abbildung 3: Chromatogramm von Cannabis der Produktgruppe II
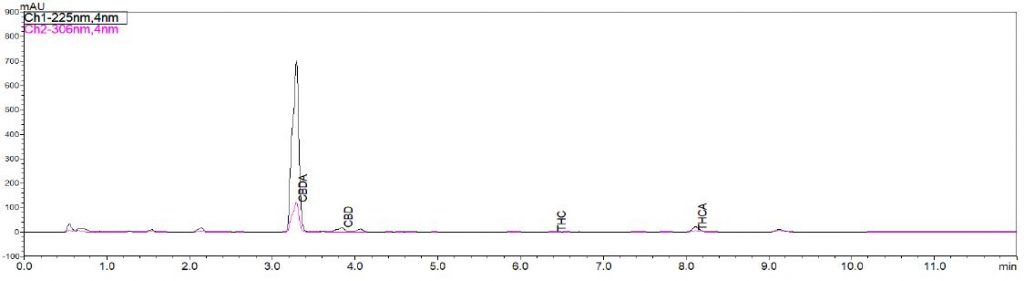
Abbildung 4: Chromatogramm von Cannabis der Produktgruppe III
| Produktgruppe I | Produktgruppe II | Produktgruppe III | ||||||
|---|---|---|---|---|---|---|---|---|
| Substanz | RT [min] | Gehalt | Substanz | RT [min] | Gehalt | Substanz | RT [min] | Gehalt |
| CBDA | 3,209 | 0,24% | CBDA | 3,288 | 6,94% | CBDA | 3,291 | 7,79% |
| CBD | 3,762 | 0,18% | CBD | 3,842 | 0,6% | CBD | 3,843 | 0,53% |
| CBN | 5,353 | 0,18% | CBN | 5,349 | 0,14% | CBN | - | - |
| THC | 6,422 | 0,99% | THC | 6,42 | 1,16% | THC | 6,417 | 0,22% |
| THCA | 8,068 | 12,54% | THCA | 8,08 | 4,66% | THCA | 8,117 | 0,71% |
| CBD-Total | 0,42% | CBD-Total | 7,54% | CBD-Total | 8,32% | |||
| THC-Total | 13,53% | THC-Total | 5,82% | THC-Total | 0,93% |
Tabelle 4: Auswertung der Messungen von Cannabis der Produktgruppen I – III (Gehaltsangaben bezogen auf Trockenmasse)
Auswertung
Die Klassifizierung der Cannabisblüten erfolgt nach dem Verhältnis des relativen Gehalts von THC zu CDB, (s. Tabelle 3) wobei die jeweilige Säureform umgerechnet und hinzugezogen wird. Zusätzlich werden die Gehalte auf die Trockenmasse bezogen.
Zusammenfassung
Die DAB Methode „Cannabisblüten“ wurde auf der i-Series Plus umgesetzt und getestet. Beispielhaft wurden 3 Proben aus allen 3 Produktgruppen erfolgreich gemessen und zuverlässig ausgewertet. Die Peakformen können durch die Co-Injektion mit Wasser weiter optimiert werden (siehe Application Note [3]).
Die den hier gezeigten Daten zugrundeliegenden Analysen wurden in den Laboren des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM), Bonn, durchgeführt.
Quellen:
[1] Deutsches Arzneibuch 2018 (DAB 2018) – Erstveröffentlichung in Bundesanzeiger Bekanntmachung BAnz AT 24.04.2018 B5
[2] EU-Richtlinie 2001/83 consolidated Version, Annex I EG
[3] Shimadzu Application Note: Optimierte Gehaltsbestimmung von Cannabis-Inhaltstoffen mittels HPLC nach DAB Monographie „Cannabisblüten“ durch Nutzung der Co-Injection
Optimierte Gehaltsbestimmung von Cannabis-Inhaltstoffen mittels HPLC nach DAB Monographie „Cannabisblüten“ durch Nutzung der Co-Injektion
Die Herstellung der Standardlösungen und die Probenaufarbeitung erfolgt mit dem in der Monographie beschriebenen Verfahren. Die Referenzlösungen und Standards werden dabei in Methanol angesetzt, während die Proben in Ethanol angesetzt werden. Dies führt zu unterschiedlichen Peakformen bei Standards und Proben. Im Fall der ethanolischen Probenextrakte ist eine verringerte Trennleistung der Säule die Folge (Abbildung 1).
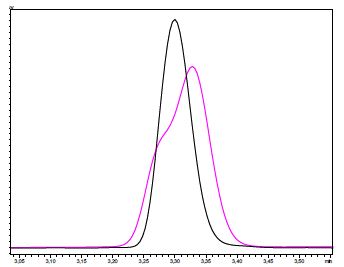
Aufgrund der Verbindlichkeit des Verfahrens darf in der pharmazeutischen Qualitätskontrolle nicht von der in der Monographie beschriebenen Probenvorbereitung und Herstellung der Standard-Lösungen abgewichen werden. Abhilfe schafft hier das Co-Injektionsverfahren, bei dem zusätzlich wenige Mikroliter Wasser aufgezogen und zusammen mit dem Standard bzw. der Probe injiziert werden.
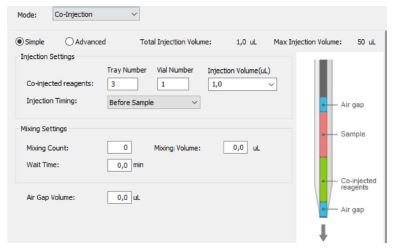
Die Co-Injektion verschiebt das Verteilungsgleichgewicht zum Zeitpunkt der Probenaufgabe kurzfristig zur stationären Phase hin, wodurch die ideale Peakform bei gleichzeitiger Verschlankung wiederhergestellt wird (Abbildung 3).
Diese Co-Injektionstechnik wird von der i-Series Plus in Verbindung mit der LabSolutions Software serienmäßig unterstützt.
Bei den hier gezeigten Co-Injektionen wurde zusätzlich zu 10μL Probenvolumen dieselbe Menge an Wasser aufgezogen.
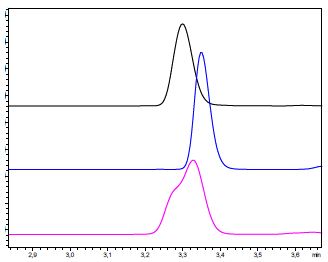
Messungen mit und ohne Co-Injektion
Zum Vergleich der DAB-Methode und der Co-Injektion wurde eine Realprobe (Cannabis der Produktgruppe 2) ohne Co-Injektion und dieselbe Realprobe mit Co-Injektion gemessen.
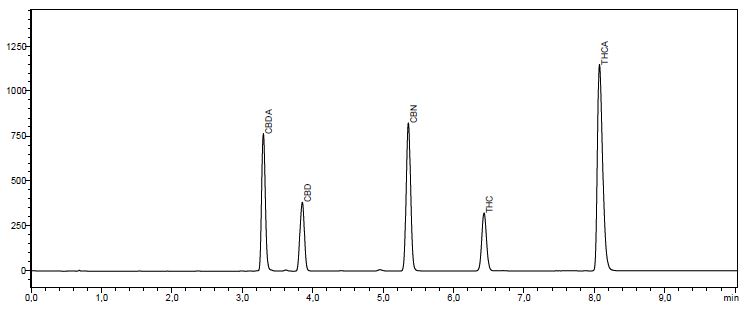
Abbildung 4: Chromatogramm eines Multistandards mit CBDA, CBD, CBN, THC und THCA
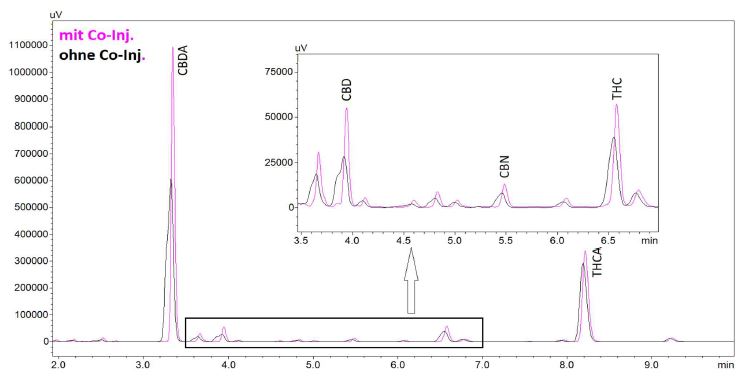
Abbildung 5: Chromatogramm einer Realprobe (Cannabis Produktgruppe II) nach DAB Monographie ohne/mit Co-Injektion
Tabelle 2: Vergleich der Peakbreiten ohne/mit Co-Injektion für obiges Chromatogramm
| Substanz | Peakbreite auf halber Höhe ohne Co-Inj. [s] | Peakbreite auf halber Höhe mit Co-Inj. [s] | Verringerung der Peakbreite um |
|---|---|---|---|
| CBDA | 5,70 | 2,70 | 52,6 % |
| CBD | 6,84 | 3,00 | 56,1 % |
| CBN | 6,12 | 3,66 | 40,2 % |
| THC | 6,06 | 3,96 | 34,7 % |
| THCA | 5,46 | 4,62 | 15,4 % |
Zusammenfassung
Durch die unterschiedlichen Lösungsmittel der Standardlösungen und der Extrakte der Cannabisblüten kommt es bei der DAB-Methode zu chromatographischen Unterschieden, die in einer schlechteren Auflösung der Realproben resultiert. Durch die Co-Injektion mit Wasser kann die Auflösung der Realproben signifikant erhöht werden und geschulterte Peaks verhindert werden. Diese Funktion ist mit der i-Series Plus und der LabSolution standardmäßig verfügbar.
Die den hier gezeigten Daten zugrundeliegenden Analysen wurden in den Laboren des Bundesinstituts für Arzneimittel und Medizinprodukte (BfArM), Bonn , durchgeführt.